| STAGNO | |
 |
 |
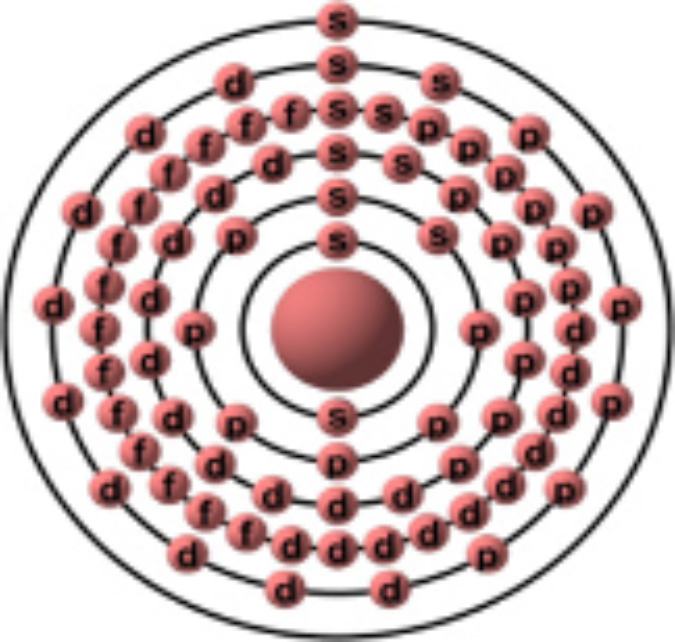
| DATI | CONFIGURAZIONE |
 |
 |
| CASSERITE | ASPETTO |
Lo stagno è un elemento chimico nella tavola periodica che ha simbolo Sn e numero atomico 50.
Questo metallo di post-transizione argenteo e malleabile, che non si ossida facilmente all’aria e resiste alla corrosione, si usa in molte leghe e per ricoprire altri metalli più vulnerabili alla corrosione. Lo stagno si ottiene soprattutto dalla cassiterite, un minerale in cui è presente sotto forma di ossido e dalla stannite.
Lo stagno è oggi il quarto metallo più prezioso dopo platino, oro e argento, ed è stato a lungo apprezzato come alternativa all’argento.
Lo stagno (dal latino stannum) è stato uno dei primi metalli ad essere scoperto, e fin dall’antichità venne intensivamente usato per il suo effetto come legante del rame, di cui aumenta di molto la durezza e le doti meccaniche formando la lega nota come bronzo, in uso fino dal 3500 a.C.

Componenti meccanici in bronzo
L’attività di estrazione mineraria dello stagno iniziò presumibilmente in Cornovaglia e a Dartmoor in età classica: grazie ad esso queste regioni svilupparono un fitto commercio con le aree civilizzate del Mar Mediterraneo. Lo stagno puro non venne usato in metallurgia fino al 600 a.C.
Le attività estrattive ebbero un’impennata verso la metà del XIX secolo dopo la scoperta delle proprietà del metallo nella conservazione dei cibi e la sua conseguente diffusione. Nel 1900 la Malaysia produceva la metà di tutto lo stagno a livello mondiale; le estrazioni erano aumentate dopo che nel 1853 l’Inghilterra aveva soppresso l’imposta su questo metallo.
Nell’epoca moderna l’alluminio ha soppiantato alcuni usi dello stagno, ma il termine “stagnola” è ancora usato per ogni metallo argenteo in forma di fogli sottili.
| PROPRIETA’ |
Lo stagno è un metallo bianco argenteo, con una struttura cristallina particolare che provoca uno stridio caratteristico quando una barra di stagno viene piegata (il rumore è causato dalla rottura dei cristalli). Possiede parecchie proprietà tra cui:
- molto malleabile;
- molto duttile (ma, se riscaldato, perde la sua duttilità e diventa fragile);
- non si ossida all’aria;
- resistente alla corrosione da acqua marina, da acqua distillata e da acqua potabile;
- agisce da catalizzatore in presenza di ossigeno disciolto nell’acqua e accelera l’attacco chimico;
- ottimo conduttore termo-elettrico;
- a-magnetico;
- alto peso specifico;
- si lega facilmente con il ferro (per questo in passato è stato utilizzato per rivestire piombo, zinco e acciaio, al fine di impedirne la corrosione).
- bassa resistenza meccanica.
| LEGHE |
Miscelando lo stagno con altri metalli si ottengono delle leghe le cui proprietà superano in molti casi quelle del metallo di origine. Le più importanti sono:
- il bronzo nelle sue varie formulazioni;
- il metallo di Babbitt, (in lingua inglese bearing metal, è una lega metallica inventata da Isaac Babbitt nel 1839 a Taunton (Massachusetts);
- leghe die casting;
- il peltro;
- la lega da saldatore;
- il princisbecco (lega di rame, zinco, stagno, simile all’oro, usata in sostituzione di questo per ricavarne fili da ricamo e laminature);
- il White metal.silumin (silicio e alluminio).
| IMPIEGHI |
Lo stagno è impiegato in molti campi come ad esempio:
- nelle saldature per unire tubi di rame e di piombo;
- nella composizione delle più diffuse leghe per saldatura utilizzate per componenti e circuiti elettronici, in leghe per bronzine,
- in una vasta gamma di processi chimici. – Il sale di stagno più importante è il cloruro di stagno che si usa come agente riducente e come mordente nella stampa calico;
- contenitori, lattine e scatolette per la conservazione dei cibi sono realizzati con una banda stagnata.
- il vetro delle finestre è molto spesso fabbricato raffreddando il vetro fuso facendolo galleggiare sopra una massa di stagno fuso (processo Pilkington – floating glass);
- quando dei sali di stagno vengono spruzzati sul vetro, si forma un rivestimento elettricamente conduttivo: questo fenomeno viene sfruttato nella fabbricazione di pannelli luminosi e per frangivento antighiaccio;
- fogli di stagno (carta stagnola) erano un imballaggio per cibo e medicinali. Ormai sono stati soppiantati da sottilissimi fogli di alluminio laminato.
 |
 |
|
| Saldatura a stagno | I famosissimi Bronzi di Riace | |
| PUOI LEGGERE ANCHE: |
| ANCHE NOI SCRITTORI | ||
 |
Alunno/i autore/i dell’articolo: | |
| GIUSEPPE PATERNÒ | ||
| Classe e Anno: | Argomento di Riferimento: | |
| Prima H – 2021/22 | METALLI | |
























 Quello prodotto con processo elettrolitico, viene definito alluminio primario, che si differenzia da quello ottenuto attraverso il riciclo detto alluminio secondario. L’alluminio ha infatti la caratteristica di poter essere riutilizzato all’infinito. Nel passato era più raro e costoso dell’oro e il riciclo ha aiutato a ridurne i costi di produzione fino al 90%. Infatti, questo metallo è estratto dall’allumina che ha una temperatura di fusione molto alta, circa 2.050°C richiedendo per questa operazione un enorme dispendio di energia che ne fa lievitare i costi.
Quello prodotto con processo elettrolitico, viene definito alluminio primario, che si differenzia da quello ottenuto attraverso il riciclo detto alluminio secondario. L’alluminio ha infatti la caratteristica di poter essere riutilizzato all’infinito. Nel passato era più raro e costoso dell’oro e il riciclo ha aiutato a ridurne i costi di produzione fino al 90%. Infatti, questo metallo è estratto dall’allumina che ha una temperatura di fusione molto alta, circa 2.050°C richiedendo per questa operazione un enorme dispendio di energia che ne fa lievitare i costi.

